В книгу, составленную румынским ученым, включены задачи, предлагавшиеся в последние годы на различных химических олимпиадах, на вступительных экзаменах в вузах. Этот сборник, содержащий нестандартные задачи, будет способствовать выработке у школьников химического мышления, интуиции и устойчивого интереса к химии.
Для учащихся, готовящихся к олимпиадам и конкурсным вступительным экзаменам, преподавателей — руководителей факультативов и химических кружков, студентов младших курсов.
Предисловие редактора перевода
Предисловие автора к русскому изданию
Предисловие к румынскому изданию
Предисловие автора к румынскому изданию
Основные условные обозначения, названия и единицы физических величин
1. Химические уравнения. Формулы неорганических соединений
Условия задач
Решения
2. Смеси. Растворы
Условия задач ТВ
Решения
3. Анализ органических соединений. Изомерия
Условия задач
Решения
4. Органический синтез
Как Решать Задачи по Химии // Задачи с Уравнением Химической Реакции // Химия Просто
Условия задач
Решения
5. Механизмы реакций органических соединений
Условия задач
Решения
6. Электролиз. Гальванические элементы
Условия задач
Решения
7. Термохимия. Химическая термодинамика
Условия задач
Решения
8. Кинетика химических реакций
Условия задач
Решения
9. Выход продуктов (степень превращения) в химических реакциях. Химическое равновесие
Условия задач
Решения
10. Ионные равновесия в растворах
Условия задач
Решения
11. Задачи разных типов
Условия задач
Решения
12. Качественные задачи
Условия задач
Ответы
Литература
Дополнительная литература
Бесплатно скачать электронную книгу в удобном формате, смотреть и читать:
Скачать книгу Задачи по химии — Будруджак П. — 1989 — fileskachat.com, быстрое и бесплатное скачивание.
Скачать djvu
Ниже можно купить эту книгу по лучшей цене со скидкой с доставкой по всей России. Купить эту книгу
Источник: obuchalka.org
Химия X10 — задачи и реакции 4+
Разработчик AppCrab указал, что в соответствии с политикой конфиденциальности приложения данные могут обрабатываться так, как описано ниже. Подробные сведения доступны в политике конфиденциальности разработчика.
Не связанные с пользователем данные
- Идентификаторы
- Данные об использовании
Конфиденциальные данные могут использоваться по-разному в зависимости от вашего возраста, задействованных функций или других факторов. Подробнее
Информация
Провайдер App Crab OOO
Размер 25,7 МБ
Совместимость iPhone Требуется iOS 10.0 или новее. iPad Требуется iPadOS 10.0 или новее. iPod touch Требуется iOS 10.0 или новее. Mac Требуется macOS 11.0 или новее и компьютер Mac с чипом Apple M1 или новее.
Как Решать Задачи по Химии // Задачи с Уравнением Химической Реакции // Подготовка к ЕГЭ по Химии
Источник: apps.apple.com
Примеры решения типовых задач

Задача. Рассчитайте тепловой эффект реакции , если значения теплот образования реагентов и продуктов составляют:



Решение. В соответствии со следствием из закона Гесса



Ответ:.
Пример 2. Вычисление изменения внутренней энергии.
Задача. Определите изменение внутренней энергии при испарении 46,8г бензола при 20 о С. Теплота испарения бензола при этой температуре составляет 30,92 кДж/моль. Пары бензола подчиняются законам идеальных газов.
Решение. Изменение внутренней энергии и тепловой эффект процесса связаны между собой соотношением

.

В соответствии с уравнением Менделеева-Клапейрона: , тогда

,

где – изменение числа моль газообразных веществ в результате процесса.
Для процесса испарения бензола

 , теплота испарения бензола равна 30,92кДж/моль, то есть,
, теплота испарения бензола равна 30,92кДж/моль, то есть,  . Тогда изменение внутренней энергии при испарении 1 моль бензола
. Тогда изменение внутренней энергии при испарении 1 моль бензола

.
Число моль бензола составляет

.

Тогда изменение внутренней энергии при испарении 48,6г бензола составляет .
Пример 3. Определение теплового эффекта реакции на основе тепловых эффектов отдельных стадий процесса.
Задача. Даны три уравнения химических реакций:
(1)  ,
, 
(2)  ,
, 
(3)  ,
,  .
.

Определите тепловой эффект реакции .

Решение. Любая сложная химическая реакция может быть представлена как алгебраическая сумма ее отдельных стадий. Нетрудно заметить, что реакция представляет собой результат комбинаций трех стадий (1) – (2) + (3). Тогда

.
Пример 4. Расчет тепловых эффектов на основе энергий химических связей. Оценка энергий химических связей на основе теплового эффекта химической реакции с учетом энергии других разрывающихся и образующихся в химической реакции связей.
Задача. Рассчитайте энергию химической связи в молекуле HBr, если известны тепловой эффект реакции  ,
, 
и энергии диссоциации молекул Н2 и Br2 .
Решение. Предположим, что процесс протекает через стадии диссоциации реагентов и образование молекулы HBr. Этот процесс можно представить совокупностью следующих стадий:
 ,
, 
 ,
, 
 ,
, 

 ,
, 
В соответствии с законом Гесса


откуда:


Таким образом, энергия связи HBr .
Пример 5. Определение знака изменения энтропии на основе структуры исходного и конечного состояний системы.
Задача. Как изменяется энтропия процесса таяния льда?
Решение. Изменение энтропии этого процесса характеризует величина


Кристаллическое состояние характеризуется высокой упорядоченностью, обусловленной структурой кристаллической решетки, в которой атомы жестко связаны между собой и имеют ограниченное число степеней свободы. Такая структура может быть представлена малым числом микросостояний. В жидком состоянии молекулы имеют большую свободу движений относительно друг друга, что обусловливает образование значительно большего числа комбинаций взаимного расположения молекул (микросостояний). Поэтому такое состояние имеет большие значения S, чем кристаллическое состояние, т.е. . Это приводит к положительному изменению энтропии.
Пример 6. Определение знака изменения энтропии процесса на основе строения реагентов и продуктов реакции.
Задача. Как изменится энтропия процесса гидрирования фенола


Решение. Как и в предыдущем примере процесса определяется разностью энтропий конечного и исходного состояний

(1)
Из двух структур C6H11OH и C6H5OH первая является более высокоорганизованной, поскольку заключает в себе большее количество химических связей и большее число структурных единиц (атомов). Поэтому 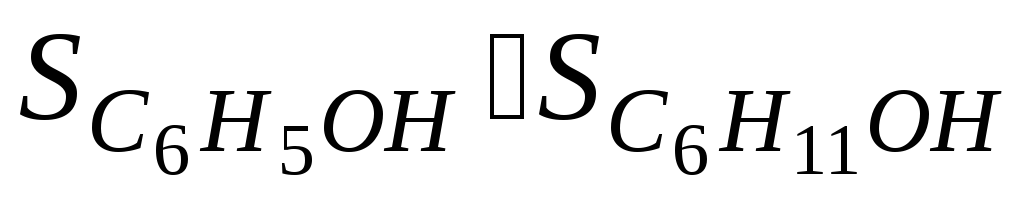 . Кроме того, второй реагент является газом, молекулы которого автономны и имеют бесчисленное множество микросостояний, поэтому
. Кроме того, второй реагент является газом, молекулы которого автономны и имеют бесчисленное множество микросостояний, поэтому  . Все это обусловливает в соответствии с (1) уменьшение энтропии при реализации процесса.
. Все это обусловливает в соответствии с (1) уменьшение энтропии при реализации процесса.
Пример 7. Выявление возможности протекания химической реакции по величине изменения энергии Гиббса.

Задача. В каком направлении будет протекать реакция в стандартных условиях?
Решение. Изменение энергии Гиббса в данной реакции характеризуется равенством

Поскольку  , то в стандартных условиях данная реакция может протекать в сторону образования
, то в стандартных условиях данная реакция может протекать в сторону образования  .
.
Пример 8. Вычисление изменение энергии Гиббса в химической реакции по значениям теплот образования и энтропий реагирующих веществ и продуктов реакции.
Задача. Вычислите изменение энергии Гиббса  для химической реакции
для химической реакции  . Возможно ли протекание этой реакции в стандартных условиях?
. Возможно ли протекание этой реакции в стандартных условиях?
Решение. Воспользуемся для решения поставленных задач значениями теплот образования и энтропий реагентов и продуктов реакции:







Изменение энергии Гиббса в химической реакции при температуре Т можно рассчитать по уравнению

.

рассчитываем на основе следствия из закона Гесса (см. ур-е 7):

 .
.
Изменение энтропии в соответствии с уравнением (6) выражается равенством:

 .
.
Изменение энергии Гиббса в химической реакции равно


Из результатов расчета () следует, что в стандартных условиях реакция осуществима.
Источник: studfile.net