N.B. Разделение на темы вопросов по химии носит приблизительный характер, так как сам формат большинства вопросов ЕГЭ по химии исключает возможность однозначного отнесения вопроса к одной определённой теме.
7929. В соответствии с термохимическим уравнением

1206 кДж теплоты выделяется при горении угля массой _____ г.
Проверить Показать подсказку

Верный ответ: 37
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 😉
При обращении указывайте id этого вопроса — 7929.
7894. В ходе реакции

выделилось 395 кДж тепла. Чему равна масса оксида серы(VI), полученного при этом?
Проверить Показать подсказку

Химия 9 класс (Урок№2 — Тепловой эффект химических реакций. )
Верный ответ: 400
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 😉
При обращении указывайте id этого вопроса — 7894.
7859. В результате реакции, термохимическое уравнение которой

выделилось 5,74 кДж теплоты. Объём (н.у.) получившегося при этом кислорода составил _____ л. (Запишите число с точностью до сотых.)
Проверить Показать подсказку

Верный ответ: 1,57
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 😉
При обращении указывайте id этого вопроса — 7859.
7824. соответствии с термохимическим уравнением

для получения 10,8 г серебра необходимо затратить теплоту в количестве ____ кДж. (Запишите число с точностью до сотых.)
Проверить Показать подсказку

Верный ответ: 15,85
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 😉
При обращении указывайте id этого вопроса — 7824.
7789. В соответствии с термохимическим уравнением
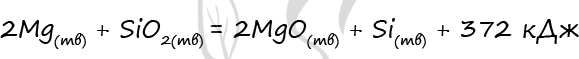
при получении 200 г оксида магния количество выделившейся теплоты будет равно _____ кДж.
Проверить Показать подсказку

Верный ответ: 930
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 😉
При обращении указывайте id этого вопроса — 7789.
7754. В соответствии с термохимическим уравнением реакции
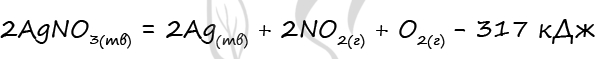
78. Тепловой эффект реакции. Термохимические уравнения (часть 1)
количество теплоты, необходимое для разложения 1,7 г нитрата серебра, составляет _____ кДж (ответ округлите до сотых).
Проверить Показать подсказку

Верный ответ: 1,59
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 😉
При обращении указывайте id этого вопроса — 7754.
7684. В реакцию, термохимическое уравнение которой
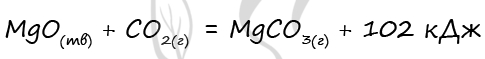
ступило 8 г оксида магния. Количество выделившейся при этом теплоты равно _____ кДж. (Запишите число с точностью до десятых.)
Проверить Показать подсказку

Верный ответ: 20,4
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 😉
При обращении указывайте id этого вопроса — 7684.
7614. В соответствии с термохимическим уравнением

для получения 2111 кДж теплоты необходимо затратить кислород объёмом (н. у.) _____ л.
Проверить Показать подсказку

Верный ответ: 120
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 😉
При обращении указывайте id этого вопроса — 7614.
7579. При окислении 4,8 г угля до оксида углерода(II) согласно уравнению

выделится теплота в количестве _____ кДж.
Проверить Показать подсказку

Верный ответ: 44
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 😉
При обращении указывайте id этого вопроса — 7579.
7544. В результате реакции, термохимическое уравнение которой

выделилось 265 кДж теплоты. Масса образовавшегося при этом оксида меди(II) равна ____ г.
Проверить Показать подсказку

Верный ответ: 80
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 😉
При обращении указывайте id этого вопроса — 7544.
Источник: studarium.ru
Ag N O 3
- Названия: Нитрат серебра(I)
 , Нитрат серебра
, Нитрат серебра
 , Адский камень
, Адский камень . показать больше Ляписный карандаш
. показать больше Ляписный карандаш , Серебра нитрат
, Серебра нитрат , Азотнокислое серебро
, Азотнокислое серебро , AgNO3
, AgNO3 показать меньше
показать меньше - Внешность (состояние): Не имеющие запаха бесцветные или белые кристаллы

Источник: chemequations.com
Задание 27. Расчёты объёмных отношений газов при химических реакциях. Расчёты по термохимическим уравнениям. ЕГЭ 2024 по химии

За это задание ты можешь получить 1 балл. На решение дается около 2 минут. Уровень сложности: базовый.
Средний процент выполнения: 65.8%
Ответом к заданию 27 по химии может быть целое число или конечная десятичная дробь.
Разбор сложных заданий в тг-канале
Задачи для практики
Задача 1
Рассчитайте массу газа, образующегося при взаимодействии с избытком кислорода 30,24 л (н. у.) оксида азота(II). (Запишите число с точностью до десятых.) Ответ в (г).
Решение
n (NO)=n($NO_2$), так как коэффициенты при веществах равны
m ($NO_2$)=1.35⋅46=62.1 г
Ответ: 62.1
Показать решение
Задача 2
В результате осуществления реакции, термохимическое уравнение которой $СаО_ + Н_2О_ = Са(ОН)_ + 70 кДж$, было получено 185 г гидроксида кальция. Вычислите количество выделившейся теплоты. (Запишите число с точностью до целых.) Ответ в (кДж).
Решение
70кДж выделяется при образовании 1моля гидроксида кальция $Са(ОН)_2$. Переходим от количества вещества к массе и получаем, что такое количество теплоты выделится при получении 1моль*74г/моль=74г гидроксида кальция. Составим пропорцию и найдем количество выделившейся теплоты: 74г — 70кДж 185г — X кДж
Ответ: 175
Показать решение
Задача 3
Какой объём (н. у.) оксида углерода(II) нужно окислить оксидом железа(II) для получения 64 л (н. у.) оксида углерода(IV)? (Запишите число с точностью до целых.) Ответ в (л).
Решение
$СО + FeО = СО_2 + Fe$
Количество вещества для газов пропорционально их объёму, поэтому отношение объёмов газов в одной реакции равно отношению их коэффициентов:
V(СО) : V($СО_2$) = n(СО) : n($СО_2$) = 1 : 1
Ответ: 64
Показать решение
Задача 4
Какой объём (н. у.) кислорода необходим для получения 80 л (н. у.) оксида углерода(IV) из угля? (Запишите число с точностью до целых.) Ответ в (л).
Решение
Количество вещества для газов пропорционально их объёму, поэтому отношение объёмов газов в одной реакции равно отношению их коэффициентов:
V($O_2$) : V($СО_2$) = n($O_2$) : n($СО_2$) = 1 : 1
Ответ: 80
Показать решение
Задача 5
В результате реакции, термохимическое уравнение которой $NH_4NO_ = N_ + 2H_2O_ + 316 кДж$, выделилось 94,8 кДж теплоты. Сколько граммов нитрита аммония вступило в реакцию? (Запишите число с точностью до десятых.) Ответ в (г).
Решение
Найдем моли реакции, разделив данное количество теплоты на количество теплоты на 1 моль:
n($NH_4NO_2$) = 94.8/316 = 0.3 моль
Найдем массу нитрита, умножив его количество на молярную массу:
m($NH_4NO_2$) = 0.3*64 = 19.2 г.
Ответ: 19.2
Показать решение
Задача 6
Какой объём кислорода необходим для окисления 46 л оксида серы(IV) в оксид серы(VI)? Объёмы газов измерены при одинаковых условиях. (Запишите число с точностью до целых.) Ответ в (л).
Решение
$2SO_2 + O_2 = 2SO_3$
Количество вещества для газов пропорционально их объёму, поэтому отношение объёмов газов в одной реакции равно отношению их коэффициентов:
V($O_2$) : V($SO_2$) = n($O_2$) : n($SO_2$) = 1 : 2
V($O_2$) = 46 : 2 = 23 л
Ответ: 23
Показать решение
Задача 7
Какой объём (н. у.) водорода теоретически необходим для синтеза 100 л (н. у.) аммиака? (Запишите число с точностью до целых.) Ответ в (л).
Решение
$N_2 + 3H_2 = 2NH_3$
Моли аммиака в реакции в полтора раза меньше моль водорода (коэффициенты 2 и 3), поэтому рассчитаем объем затраченного водорода:
$V(H_2) = 100 ⋅ 1.5 = 150$ л.
Ответ: 150
Показать решение
Задача 8
В соответствии с термохимическим уравнением реакции
2Mg(тв.) + O2(г) = 2MgO(тв.) + 1200 кДж выделилось 360 кДж теплоты.
Рассчитайте массу полученного оксида магния. (Запишите число с точностью до целых.) Ответ в (г).
Решение
По уравнению реакции находим количество вещества MgO:
x = 2 · 360 / 1200 = 0.6 моль MgO.
Находим массу MgO:
M(MgO) = 40 г/моль; m(MgO) = 0.6 · 40 = 24 г
Ответ: 24
Показать решение
Задача 9
Какой объём хлора (объёмы газов измерены при одинаковых условиях) теоретически вступает в реакцию с 56 л водорода? (Запишите число с точностью до целых.) Ответ в (л).
Решение
Основные формулы для расчёта:
$n = V_г /V_M$; $n = m_ / М_$
1) Составляем уравнение реакции:
2) Логическая связь:
Требуется найти объём хлора, расчёт будем производить по количеству вещества водорода.
3) Расчёт по уравнению реакции.
Только для расчёта объёма реагирующих газов:
объёмы реагирующих газов относятся как коэффициенты в уравнении реакции:
$V(H_2) / 1 = V(Cl_2) / 1$
Ответ: 56
Показать решение
Показать еще
Необходимо зарегистрироваться
Для доступа к решениям необходимо включить уведомления от группы Турбо в вк — это займет буквально 10 секунд. Никакого спама, только самое важное и полезное для тебя. Ты всегда можешь запретить уведомления.
Подпишись на полезные материалы ЕГЭ по химии: разбор реальных вариантов ЕГЭ и сложных заданий + авторские конспекты
Источник: egeturbo.ru